Haloformová reakce
- Cíl pokusu
-
prokázat charakteristické skupiny v molekule alkoholů vedoucí k haloformům
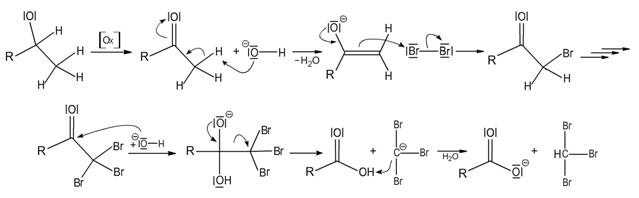
Podle autora bývá haloformová reakce také nazývána jako Liebenova. Reakce probíhá v zásaditém prostředí se sloučeninami s methylovou skupinou navázanou vedle hydroxylové, či karbonylové skupiny.
V prvním kroku nejprve dojde k oxidaci alkoholu na keton. V zásaditém prostředí dojde k odtržení vodíku z methylové skupiny a vzniku enolátu. Působením halogenu (Cl2, Br2, I2) se postupně vytvoří trihalogenmethylketon. Tento meziprodukt je velice náchylný k nukleofilní adici hydroxylového aniontu na karbonylovou skupinu díky silnému působení indukčního efektu trihalogenmethylové skupiny. Meziprodukt se následně rozpadne na sůl karboxylové kyseliny a tzv. haloform.
Tato reakce se využívá při přípravě karboxylových kyselin, chloroformu, bromoformu, jodoformu a také jako důkazová reakce pro přítomnost ethanolu. Ten je tímto způsobem průkazný ještě při koncentraci 0,05 %
- Použité chemikálie
-
-
isopropanol – F (hořlavý)
-
jod – Xi (dráždivý), N (nebezpečný pro životní prostředí)
-
roztok hydroxidu sodného – C (žíravý)
-
- Postup
-
V kádince vytvoříme roztok jodu v isopropanolu. Několik ml tohoto roztoku nalijeme do zkumavky a po kapkách k němu přidáme takové množství roztoku hydroxidu sodného, dokud nedojde k úplnému odbarvení reakční směsi.
- Pozorování
-
Ve zkumavce v průběhu reakce začne roztok měnit barvu ze sytě oranžové na zelenou. Při oxidaci ethanolu probíhá zároveň redukce šestimocného chromu s typicky oranžovou barvou na chrom trojmocný (chromité ionty), pro něhož je typické zelené zbarvení.
- Závěr
-
Smícháním isopropanolu a jodu získáme sytě oranžový roztok. Po zalkalizování reakční směsi přidáním hydroxidu sodného začne probíhat reakce a velice rychle dojde k odbarvení roztoku a vyloučení světle žlutého jodoformu.