1.3.1 Přehled názvů skupin a podskupin prvků
V současné době přežívají tradiční skupinové názvy uvedené v tabulce Va. Zařazení prvků do těchto skupin však v mnohých případech nebralo ohled na elektronovou konfiguraci prvků (např. ke kovům alkalických zemin nejsou zařazovány prvky Be, Mg, přestože se vyznačují elektronotou konfigurací ns2, obdobně jako Ca, Sr, Ba, Ra).
Tabulka Va: Tradiční skupinové názvy prvků
| alkalické kovy | Li, Na, K, Rb, Cs, Fr |
| kovy alkalických zemin | Ca, Sr, Ba, Ra |
| chalkogeny | O, S, Se, Te, Po |
| halogeny | F, Cl, Br, I, At |
| vzácné plyny | He, Ne, Ar, Kr, Xe, Rn |
| prvky vzácných zemin | Sc, Y, La, Ce až Lu |
| lanthanoidy | Ce až Lu |
| aktinoidy | Th až Lr |
| transurany | Np až Lr |
| triáda železa | Fe, Co, Ni |
| lehké kovy platinové | Ru, Rh, Pd |
| těžké kovy platinové | Os, Ir, Pt |
Nově byly zavedeny tyto skupinové názvy (tabulka Vb):
Tabulka Vb: Nově zavedené skupinové názvy prvků
| triely | B, Al, Ga, In, Tl |
| tetrely | C, Si, Ge, Sn, Pb |
| pentely | N, P, As, Sb, Bi |
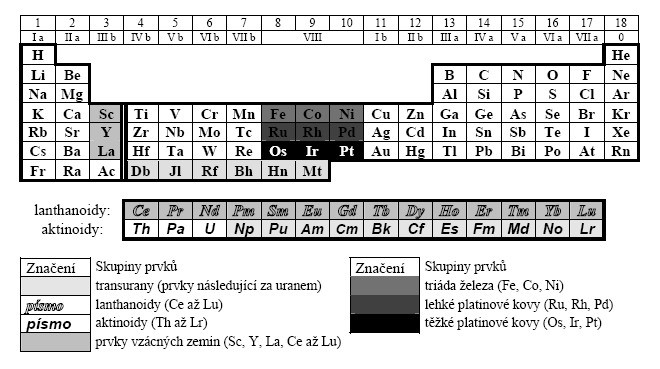
Výše uvedené skupiny prvků znázorňuje obrázek 2.
Obr. 2: Skupinové názvy prvků
- alkalické kovy, kovy alkalických zemin, triely, tetrely, pentely, chalkogeny, halogeny, vzácné plyny
- transurany, lanthanoidy, aktinoidy, prvky vzácných zemin, triáda železa, lehké platinové kovy, lehké platinové kovy, těžké platinové kovy
Pozn.: Značení skupin:
IUPAC, Nomenclature of Inorganic Chemistry, 1989: 1, 2, …, 17, 18
IUPAC, Rules for Inorganic Nomenclature, 1970: I a, II a, … I b, II b,…
Obr. 2a

Obr. 2b
Nověji se prvky člení do skupin podle elektronové konfigurace jejich valenční vrstvy. Skupiny prvků se označují římskými číslicemi 0, I, II, … VIII nebo arabskými číslicemi 1, 2, 3, …, 18 (obr. 3).
Obr. 3: Označení skupin v periodické soustavě prvků

Dále lze skupiny prvků členit na podskupiny. Podskupiny prvků se označují přiřazením tiskacích písmen A a B (případně a, b) k římské číslici označující skupinu (obr. 3). Podskupiny A (případně a) bývají označovány jako hlavní, podskupiny B (případně b) jako vedlejší. Podskupiny prvků podobných vlastností je možno označovat i názvem prvního prvku podskupiny, např. prvky podskupiny manganu (Mn, Tc, Re), prvky podskupiny chromu (Cr, Mo, W), prvky podskupiny vanadu (V, Nb, Ta), prvky podskupiny titanu (Ti, Zr, Hf, Db)…
Podle doporučení IUPAC z roku 1970 jsou do podskupin A (a) řazeny prvky nepřechodné, do podskupin B (b) prvky přechodné. V české odborné literatuře (např. [7], jejíž autor je zároveň členem české názvoslovné komise), se však používá i jiné členění prvků do podskupin A, B, které znázorňuje tabulka VI. Nověji je možno členit periodickou tabulku na skupiny označované 1, 2, 3, …, 18 (obr. 3), kde každé podskupině je přiděleno její samostatné číslo (IUPAC, 1989).
Tabulka VI: Alternativní označování podskupin A, B
| 1A | 2A | 3A | 4A | 5A | 6A | 7A |
| K | Ca | Sc | Ti | V | Cr | Mn |
| 1B | 2B | 3B | 4B | 5B | 6B | 7B |
| Cu | Zn | Ga | Ge | As | Se | Br |
Prvky lze dělit dle vlastností na kovy, nekovy a polokovy, popř. na nepřechodné prvky (s-a p-prvky), prvky přechodné (d-prvky) a prvky vnitřně přechodné (f-prvky), jak je znázorněno na obr. 4.
**včetně aktinoidů, avšak thorium, protaktinium a uran jsou v některých literárních pramenech řazeny do podskupin 4A, 5A, 6A
Obr. 4: Členění prvků na s-prvky, p-prvky, d-prvky, f-prvky

PdF, Pedagogická fakulta, Masarykova univerzita
Návrat na úvodní stránku webu, nahoru
Technická spolupráce:
Servisní středisko pro e-learning na MU
Fakulta informatiky Masarykovy univerzity, 2009
