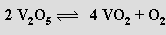
Oxid vanadičný V2O5 je oranžová krystalická látka s amfoterními vlastnostmi, která se připravuje z metavanadičnanu amonného NH4VO3 (produkt připravený spalováním kovu v nadbytku kyslíku je vždy kontaminován nižšími oxidy). Jeho struktura je složitá a sestává ze silně deformovaných trigonálních bipyramid VO5 spojených hranami do dvojitých lomených řetězců. Při zvýšené teplotě (700 až 1125 °C) se oxid vanadičný vratně rozkládá
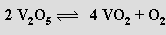
Toto chování je příčinou jeho katalytických schopností využívaných pro oxidaci oxidu siřičitého na oxid sírový při výrobě kyseliny sírové. Rozpuštěním oxidu vanadičného v kyselině sírové vzniká síran dioxovanadičný (VO2)2SO4, jehož redukcí lze připravit síran vanadylu (+2) VOSO4 jako pentahydrát i bezvodou sůl. Redukcí za zvýšené teploty lze z oxidu vanadičného připravit řadu (třináct) nižších oxidických fází. Oxidy niobičný Nb2O5 a tantaličný Ta2O5 jsou rovněž amfoterní, redukci podléhají méně ochotně než oxid vanadičný. Oba oxidy tvoří několik polymorfních modifikací se složitými strukturami.
Použije-li se k redukci oxidu vanadičného oxid uhelnatý nebo siřičitý, je produktem modročerný oxid vanadičitý VO2, redukce vodíkem poskytne šedočerný oxid vanaditý V2O3 až šedý oxid vanadnatý VO. Oxidy M2O3 nejsou u niobu a tantalu známy. Zřetelně menší tendenci k tvorbě nižších oxidů projevuje tantal (existence oxidu tantalnatého TaO nebyla zatím potvrzena). Všechny tři prvky tvoří značný počet sulfidů, selenidů a telluridů, ale často s odlišnou stechiometrií (V3S, V5S4 , V7S8, V3S4) i strukturou než mají oxidy.
Jediným známým pentahalogenidem VV je fluorid vanadičný VF5 se strukturou řetězovitého polymeru, zatímco u niobu a tantalu jsou známy kompletní řady pentahalogenidů. Všechny lze připravit přímou reakcí prvků. Fluorid niobičný NbF5 a fluorid tantaličný TaF5 tvoří tetramerní molekuly, chlorid niobičný NbCl5 a bromidy niobičný NbBr5 i tantaličný TaBr5 jsou dimery složené ze dvou deformovaných oktaedrů spojených hranou; v plynné fázi jsou všechny monomerní. Jsou silnými Lewisovými kyselinami (schopnost tvořit adukty D.MX5 (D = donor) klesá s rostoucí hmotností halogenu X), které lze redukovat na tetrahalogenidy MX4 (k jejich přípravě je použitelná i reakce prvků za kontrolovaných podmínek).
|
Struktura (MF5)4 (M = Nb, Ta)
|
Struktura (MX5)2 (M = Nb, Ta; X = cl, Br)
|
Fluorid vanadičitý VF4 je světle zelená látka se sklonem k disproporcionaci
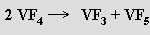
Červenohnědý kapalný chlorid vanadičitý VCl4 je obsahuje tetraedrické molekuly a vodou se rychle hydrolyzuje na dichlorid vanadylu VOCl2. Na rozdíl od fluoridu vanadičitého se termicky místo disproporcionace rozkládá na chlorid vanaditý a chlor (stejně se chová i bromid vanadičitý VBr4)
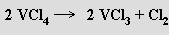
Tetrahalogenidy niobu a tantalu jsou pevné polymerní, proti očekávání diamagnetické látky.
Halogenidy vanadité jsou barevné krystalické polymery, v nichž má vanad koordinační číslo šest. Fluorid vanaditý VF3 je dostupný fluorací chloridu vanaditého suchým fluorovodíkem (s vodou poskytuje trihydrát, ostatní trihalogenidy tvoří hexahydráty) a z halogenidů vanaditých je nejstálejší vůči oxidaci vzdušným kyslíkem. Chlorid vanaditý VCl3 vzniká termickým rozkladem chloridu vanadičitého nebo zahříváním vanadu v proudu suchého chlorovodíku
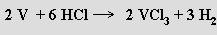
Bromid vanaditý VBr3 a jodid vanaditý VI3 se tvoří reakcí prvků.
Všechny halogenidy vanadnaté VX2 jsou hygroskopické a mají silné redukční účinky. V jejich levandulově zbarvených vodných roztocích jsou přítomny nestálé kationty [V(H2O)6]2+. Chlorid vanadnatý VCl2 lze připravit disproporcionací chloridu vanaditého
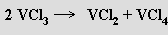
Halogenidy MX2 (M = Nb, Ta) nejsou známy, existují však klastrové sloučeniny MX2,33 (diamagnetické sloučeniny Nb6Cl14 a Ta6Cl14 lze považovat za dichloridy komplexních kationtů [M6 Cl12]2+) a MX2,5 (paramagnetické) stabilizované vazbami kov-kov.
Oxid-halogenidy vanadu existují pouze v oxidačních stavech +III a +V. Oxidací fluoridu vanaditého kyslíkem je dostupný trifluorid vanadylu VOF3
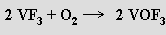
Trichlorid vanadylu VOCl3 se tvoří reakcí chlorovodíku s oxidem vanadičným za přítomnosti oxidu fosforečného, který váže vznikající vodu
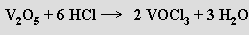
nebo zahříváním oxidu vanadičného s uhlíkem v proudu chloru
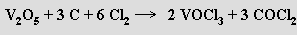
Dichlorid vanadylu VOCl2 vzniká jeho redukcí vodíkem
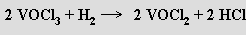
nebo hydrolýzou chloridu vanadičitého
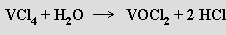
Polymerní oxid-halogenidy MOX3 (M = Nb, Ta) lze připravit reakcemi
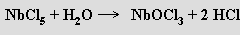
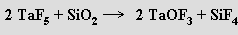
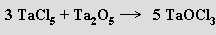
U niobu a tantalu existují i halogeniddioxidy MO2X. Halogenidy a halogenidoxidy obou prvků tvoří rozmanité komplexy s vysokými koordinačními čísly kovů (anion [TaF8]3− má tvar čtvercového antiprizmatu)
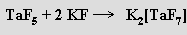
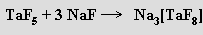
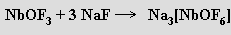
V roztocích hydroxidů alkalických kovů (při pH > 13) se oxid vanadičný rozpouští na bezbarvé orthovanadičnany (krystalují jako hydráty Na3VO4.12H2O, K3VO4.6H2O), v nichž je vanad koordinován tetraedricky. Při snižování hodnoty pH dochází ke kondenzačním reakcím za vzniku hydrogenvanadičnanů HVO42−, divanadičnanů V2O74−, hydrogendivanadičnanů HV2O73− (pH 9-13)
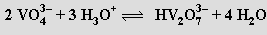
až metavadičnanů (VO3)nn− (pH 8-9). Při přechodu do kyselé oblasti převládají dihydrogendekavanadičnany [H2V10O28]4− složené z kondenzovaných oktaedrů VO6
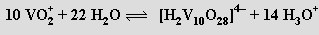
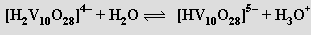
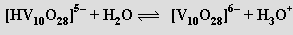
V isoelektrickém bodě (pH = 2,2) se sráží hydratovaný oxid vanadičný, při dalším snižování pH se opět rozpouští za vzniku kationtů VO2+. Zbarvení polyvanadičnanů se prohlubuje se stupněm kondenzace (soli kationtu VO2+ jsou žluté, trivanadičnan amonný je zbarvený zlatě a pentavanadičnan draselný je tmavočervený). U niobu a tantalu je stechiometrická rozmanitost izopolyaniontů mnohem menší než u vanadu. Při pH < 11 se v roztoku předpokládá přítomnost aniontů M6O198− (M = Nb, Ta). Izoelektrický bod, v němž dochází ke srážení nerozpustných hydratovaných oxidů, leží při vyšším pH než u vanadu (sedm pro niob a deset pro tantal).
S peroxidem vodíku poskytují vanadičnany intenzivně zbarvené peroxokomplexy. V alkalickém a netrálním prostředí vznikají žluté anionty dioxodiperoxovanadičnanové [VO2(O2)2]3− (známy jsou i modrofialové tetraperoxovanadičnany [V(O2)4]3−), v kyselých roztocích se tvoří červenohnědé kationty peroxovanadičné [V(O2)]3+. Podobné peroxosloučeniny jsou známy i u niobu a tantalu.
Organokovové sloučeniny reprezentují především karbonylové ([V(CO)6]), kyanidové a cyklopentadienylové komplexy (je znám nestálý sendvičový vanadocen, jeho strukturní ekvivalenty u niobu a tantalu neexistují), málo je známo o alkyl- a arylsloučeninách všech tří prvků 5. skupiny.