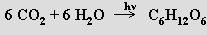
Lithium je stopovým biogenním prvkem, který se již v minulém století využíval k léčení kloubních onemocnění. Jeho nedostatek v lidském organismu je příčinou některých psychických chorob, uhličitan lithný se s úspěchem používá k léčení depresivních a agresivních stavů, narkomanie a alkoholismu. Sloučeniny lithia působí i proti skleróze, vysokému krevnímu tlaku, cukrovce a příznivě ovlivňují i krvetvorný systém včetně kostní dřeně. Zdrojem lithia jsou minerální vody a některé druhy rostlin (obsah lithia je v různých částech rostliny různý a význam má i doba sběru).
Průměrný obsah sodíku v lidském těle je 70 až 105 gramů. Jeho rozložení je nerovnoměrné, nejvíce ho je v mimobuněčných tekutinách (krevní plazmě), třetina je uložena jako uvolnitelná zásoba v kostech. Sodík udržuje v tkanivovém moku vhodný osmotický tlak a účastní se transportu glukózy a aminokyselin buňkovými membránami. Do organismu se dostává potravou většinou ve formě chloridu sodného (zachytí se 95 % přijímaného sodíku, reálná potřeba je 2 až 5 gramů denně). Nadbytek sodíku vyvolává poruchy vodního hospodářství těla (zvyšuje krevní tlak a obsah vody v organismu způsobující otoky, je také jednou z příčin anemie). Naopak jeho nedostatek je příčinou únavy, bolestí hlavy, depresí , svalových křečí a při déletrvajícím nedostatku nastává oběhový kolaps. Vylučování regulují ledviny, velké ztráty mohou nastat nadměrným pocením a při onemocněních provázených zvracení a průjmy. Vysoký obsah sodíku je v uzeninách, konzervované zelenině a sýrech, v menším množství je obsažen v rýži, mouce, tucích, zelenině a ovoci.
Draslík je v lidském těle zastoupen ještě více než sodík (140 až 175 g). 80 % se ho nachází ve svalových buňkách, zbytek v tělních tekutinách a zanedbatelné množství v kostech. Většinou je vázán na bílkoviny a významně se podílí na procesech kontrakce svalů, přenosu nervových vzruchů a metabolismu sacharidů i bílkovin. Denně člověk potřebuje v potravě přijmout přibližně 5 g draslíku (zachycuje se až 90 % přijímaného prvku). Nedostatek i nadbytek draslíku se projevují téměř stejně celkovou slabostí, poruchami srdeční činnosti a centrální nervové soustavy. Zdrojem draslíku jsou ovoce a zelenina, mléko, maso a droždí. Draslík je velmi důležitý pro rostliny a omezení jeho přívodu se užívá k hubení plevele.
Hořčík je využíván v rostlinách jako součást komplexů, které hrají klíčovou roli při fotosyntéze, kterou lze sumárně (ve velmi hrubém zjednodušení) vyjádřit rovnicí
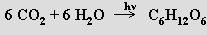
Proces je základem výživy živých organismů (90 až 95 % hmotnosti obilí vzniká fotosyntézou a pouze 5 až 10 % je minerálního původu) a jeho produkty jsou i fosilní paliva (dřevo, uhlí, ropa). Fotosyntéza je zahajována ve fotoreceptorech se zelenými pigmenty obsahujícími hořčík, které se nazývají chlorofyly (chloros = zelený, fylon = list). Celkový děj je silně endotermní (ΔH°= 469 kJ.mol-1 CO2), účastní se jej několik typů chlorofylu, manganatý komplex neznámého složení, cytochromy, ferredoxin a plastocyanin. Řada jeho na sebe navazujících kroků může probíhat i bez osvětlení. Světelná energie je tímto způsobem přeměňována na energii chemickou uloženou v adenosintrifosfátu (ATP) a redukovaném nikotinamidadenindinukleotidfosfátu (NADP), která umožňuje endotermní přeměnu oxidu uhličitého a vody na cukry za uvolnění kyslíku. Strukturou jsou chlorofyly (známy jsou čtyři varianty rozlišované písmeny a až d, a je nejběžnější a nachází se ve všech organismech schopných fotosyntézy, b je součástí vyšších rostlin a zelených řas, c je obsažena v rozsivkách a hnědých řasách) blízce příbuzné hemu. V obou případech je makrocyklický ligand odvozen od mateřské molekuly porfinu, modifikace obsažená v chlorofylech se nazývá chlorin. Koordinační číslo hořčíku v chlorinovém komplexu je pět (někdy šest) a zejména voda jako další ligand hraje důležitou úlohu při spojování chlorofylů do rozsáhlejších útvarů (konglomeráty o délce 1500 až 2000 pm), které se účastní procesu fotosyntézy. V jejím průběhu je dvěma následně probíhajícími fotoprocesy absorbováno světlo z červené oblasti (680-700 pm). Hořčík přitom pevností své vazby k makrocyklickému ligandu zamezuje rozptýlení energie termickými vibracemi a zvyšuje rychlost přechodu nestabilního excitovaného singletového stavu na stabilnější tripletový stav, v němž se pak komplex účastní dalšího redoxního děje. Není dosud známo, proč je hořčík jediným k těmto účelům vhodným kovem. Hořčík je nutný i k aktivaci enzymů přenášejících fosforečnany a významně ovlivňuje i hydrolytické procesy, při nichž se z adenosintrifosfátu (ATP) tvoří adenosindifosfát (ADP) a adenosinmonofosfát (AMP) a uvolňuje se značné množství energie potřebné k realizaci biochemických procesů
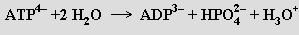
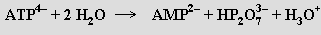
Vápník byl už krátce po svém objevu identifikován jako součást kostí, zubů a chrupavek u savců, kde je obsažen ve formě hydroxyl- nebo karbonátoapatitu. Nejde o neměnnou neživou formu existence kationtů vápenatých, protože existuje dynamická rovnováha mezi těmito částmi těla a tělními tekutinami (kosti se neustále rozpouštějí a znovu vytvářejí), jejíž poruchy mohou vést k dekalcinaci kostí (osteoporosa). Je proto třeba trvalý přívod tohoto prvku v potravě (pro dospělého člověka 1 gram denně; resorpce z potravy není příliš efektivní). V rostlinách se vápník vyskytuje ve větší míře mimo buňky a podobně jako u savců má především zpevňující funkci. V živočišných organismech se vápní k účastní ještě řady dalších procesů. Společně se sodíkem se podí lí na ustavování membránových rovnováh a v této funkci je považován za univerzální regulátor buněčných funkcí (mimo buňky je koncentrace vápníku velmi stabilní a podstatně větší než uvnitř buněk). Podílí se i na procesech kontrakce svalů, neuronových vzruchů a vidění. Významnou roli hraje v metabolismu glukózy (při její syntéze i degradaci) a při srážení krve. Zvyšuje tepelnou odolnost bílkovin a je součástí řady enzymů (zřídka však v nich představuje vlastní aktivní centrum). Také intenzita bioluminiscence světélkujících organismů je řízena změnou koncentrace vápníku.