Zařízení
Plynový kahan
Plynové kahany jsou laboratorní zařízení, která se skládají z podstavce, z kterého ústí trubice pro přívod plynu. Ve spodní části je šroub k regulaci přívodu plynu a vzduchu. Plyn jde až k otvoru pro vzduch a společně stoupají hořákovou trubicí vzhůru, kde hoří.
Existují různé druhy kahanů jako je Bunsenův, Tecluho a Mekerův, které se odlišují svou konstrukcí. Pomocí různých typů kahanů dosáhneme rozdílných maximálních teplot a tvaru plamene. Nejchladnější plamen má Bunsenův kahan a nejteplejší Mekerův. (3), (5)
Plamen kahanu nemá všude stejnou teplotu. Rozlišujeme proto dva sektory podle barvy a teploty plamenu. Chladné tmavé jádro je část plamene, která se označuje jako redukční kužel a obsahuje nespálenou směs vzduchu a plynu. Skládá se také z nesvítivého obalu, ve kterém dojde k dokonalejšímu spalování a tím i k dosažení vyšší teploty. Zvětšením přívodu vzduchu do kahanu se kužel zkracuje. Může dojít i k tzv. zaskočení plamene a směs začne hořet uvnitř kahanu. Viditelně se to projeví zezelenáním plamene a kahan začne vydávat charakteristický chrčivý zvuk. Za těchto okolností je nutné kahan zavřít přívod plynu a nechat kahan vychladnout. (3), (5)

Váhy
Vážení je jedna z nejzákladnějších metod prováděných v chemické laboratoři, proto jsou nezbytnou součástí laboratoře kvalitní váhy. Mohou být mechanické nebo dnes častěji používané digitální. Váhy dělíme podle kritéria váživosti (maximální hmotnost, kterou váha zváží) a podle citlivosti neboli přesnosti vah na váhy technické (předvážky) a na analytické. Veškeré váhy (především analytické) musíme udržovat v maximální čistotě, abychom zaručili jejich správnost fungování. Z toho důvodu by měly být v čistém prostředí s menší vlhkostí bez průvanu, otřesů a se stabilní teplotou. (3), (5)


Vážení na digitálních vahách je méně náročné než na mechanických. Pozor musíme dát na maximální hmotnost, kterou lze na vahách zvážit. Na váhy umístíme prázdnou nádobu, do které budeme danou látku vážit a zmáčkneme tlačítko „Tare“, tím na vahách nastavíme nulovou hodnotu. Poté už můžeme do nádoby vkládat požadované množství látky. (3)
Teploměry
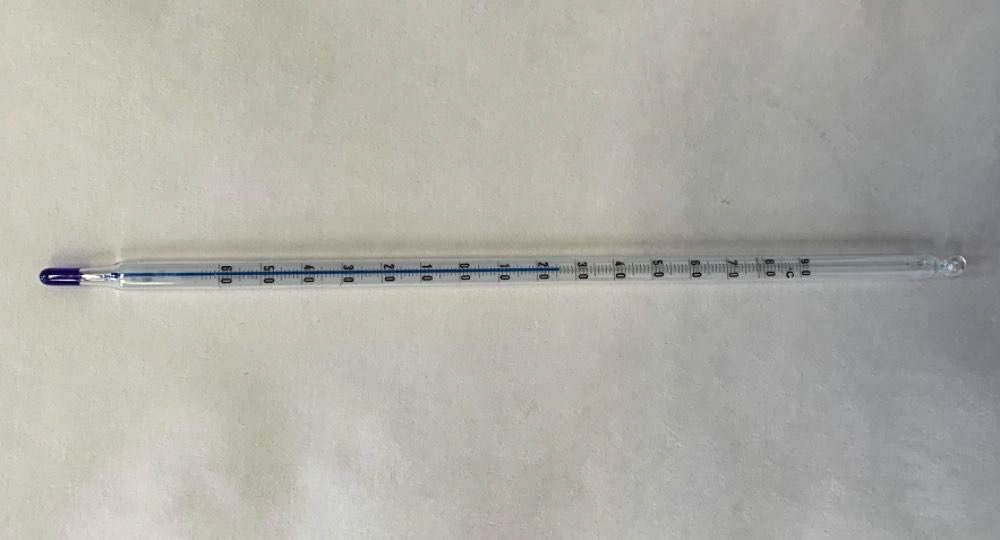
Ke stanovení teploty reakční směsi slouží teploměry. Dříve se používaly teploměry především rtuťové, dnes se používají vhodná organická rozpouštědla, která jsou pro lepší odečítání hodnot obarvena modře nebo červeně. Skleněné teploměry jsou plněny alkoholem (rozsah od –200 do 78 °C, rozsah je závislý na druhu alkoholu) nebo rtutí (rozsah od –37 do 356 °C) a také se v laboratoři setkáváme s digitálními teploměry. V destilačních aparaturách se běžně používají zábrusové teploměry, které se vsouvají do Claisenova nádstavce.
Rotační vakuová odparka
Rotační vakuová odparka je laboratorní zařízení, které slouží k rychlému odpaření velkého množství rozpouštědla a získání pevné (nebo netěkavé kapalné) látky. Skládá se z baňky, která je připojena na přívod vakua. Baňka obsahující roztok vzorku rotuje a tím se zvětší povrchová plocha vzorku. Dojde k urychlení odpařování těkavější složky (rozpouštědla), a zároveň se zpravidla se sníží bod varu vlivem snížení tlaku. Toto zařízení se používá při destilaci za sníženého tlaku, zahušťování, vysoušení nebo při krystalizaci.

Refraktometr
Refraktometr je přístroj, který slouží ke stanovení indexu lomu. Nejpoužívanějším typem je Abbeho refraktometr, kterému stačí k měření pouhá kapka vzorku, ta se kápne mezi dva hranoly. (6)

Bodotávky
Bodotávky jsou zařízení, které se používají ke stanovení teploty tání. Je to elektricky vyhřívaná plotýnka ve spojení s mikroskopem a teploměrem. Když necháváme látku tát, můžeme ji pozorovat mikroskopem, kterým vidíme i teploměr. Výhodou je, že nám ke stanovení teploty tání postačí velmi malé množství látky (několik krystalků), z toho důvodu můžeme pracovat v mikro až v submikroměřítku (miligramy až mikrogramy). (6)

Pomocí bodotávku nezjistíme přesnou hodnotu teploty tání vzorku, ale rozmezí teplot, ve kterém vzorek taje. Zaznamenáváme dvě teploty, nejprve tu, při které se začínají krystaly vzorku bortit a jako druhou teplotu, při které je celý objem vzorku kapalný.
Magnetické míchačky
V první řadě je nutné rozlišovat dva pojmy. Míchačka je přístroj, na rozdíl od míchadla, což je součástka, jejíž pohybem způsobíme míchání. Magnetické míchačky dnes často slouží nejen k míchání, ale i k zahřívání vzorku. Existují i míchačky s více místy pro vzorky. (6)

NMR spektrometr
Nukleární magnetická rezonance (NMR) je metoda, která umožňuje kvantitativní a kvalitativní analýzu vzorku. Na obrázku je stolní (benchtop) NMR spektrometr, který umožňuje měřit jádra 1H a 19F. Rezonanční frekvence jader 1H je 60 MHz. Součástí spektrometru je permanentní magnet, který nevyžaduje chlazení kryokapalinami.
Vzorek se do magnetu vkládá v 5 mm skleněné kyvetě, pro měření není nutné (na rozdíl od klasických NMR spektrometrů se supravodivým magnetem) použít deuterované rozpouštědlo.



Infračervený spektrometr
Infračervená spektroskopie je metoda kvalitativní a kvantitativní analýzy, studuje absorpci infračerveného záření vzorkem. Na snímku je spektrometr umožňující měření v reflexním módu metodou zeslabeného úplného odrazu (ATR – Attenuated Total Reflectance)
Při této měřící technice není nutné vzorek nijak upravovat, pouze se umístí na krystal (nejčastěji z diamantu) a v případě pevné látky se přitlačí pomocí hrotu. Kapaliny měříme bez přítlaku.


Plynový chromatograf
Plynový chromatograf je zařízení určené k separaci a identifikaci směsí. Kapalná směs je injektována do kolony umístěné v temperovaném prostoru. Kolona je naplněna stacionární fází, nejčastěji silikagelem, vzorek je kolonou unášen pomocí mobilní fáze (nosného plynu). Na koloně dochází k separaci složek směsi, separované složky jsou z kolony unášeny k detektoru, který umožňuje určení identity a kvantity složek.

3. UNIVERZITA PALACKÉHO V OLOMOUCI Přírodovědecká fakulta Katedra fyzikální chemie LABORATORNÍ TECHNIKA PETR SUCHOMEL, MICHAL OTYEPKA - PDF [Internet]. [citován 29. prosinec 2018]. Dostupné z: https://docplayer.cz/11100856-Univerzita-palackeho-v-olomouci-prirodovedecka-fakulta-katedra-fyzikalni-chemie-laboratorni-technika-petr-suchomel-michal-otyepka.html
5. Alonž (chemie). In: Wikipedie [Internet]. 2016 [citován 30. prosinec 2018]. Dostupné z: https://cs.wikipedia.org/w/index.php?title=Alon%C5%BE_(chemie)&oldid=13526898
6. ELUC [Internet]. [citován 6. leden 2019]. Dostupné z: https://eluc.kr-olomoucky.cz/verejne/lekce/2256