Vlastnosti aminů
- Cíl pokusu
-
Demonstrovat vlastnosti aromatických aminů - anilinu.
- Chemikálie
-
-
anilin - T (toxický), N (nebezpečný pro životní prostředí
-
kyselina chlorovodíková (w = 35 %) - C (žíravá)
-
hydroxid sodný (w = 40 %) - C (žíravý)
-
bromová voda - T+ (vysoce toxický), C (žíravý), N (nebezpečný pro životní prostředí)
-
- Postup
-
Ve zkumavce smícháme 0,5 ml anilinu a 5 ml vody. Utvoří se 2 fáze. Po přidání několika kapek HCl vznikne čirý roztok. Jeho zalkalizováním vzniknou opět dvě vrstvy - anilin a vodný roztok NaCl.
V kádince rozpustíme 0,5 ml anilinu v 30 ml vody. Vznikne roztok anilinu ve vodě (anilinová voda). Přibližně 10 ml tohoto roztoku nalijeme do zkumavky. Přidáme několik kapek bromové vody. Vzniká sraženina.
- Pozorování
-
Anilin je slabá báze a zapojuje volný elektronový pár na dusíku do konjugace s aromatickým jádrem.
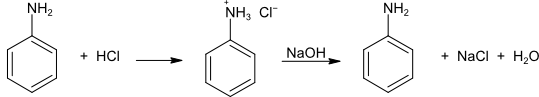
Díky kyselině chlorovodíkové dochází k protonizaci a tvorbě amoniové soli - rozpustné soli ve vodě (čirý roztok). Přidáním roztoku hydroxidu sodného dochází k tvorbě stabilnější soli - chloridu sodného - a opětovnému převedení amoniové soli na amin a rozdělení vrstev anilinu a vody.
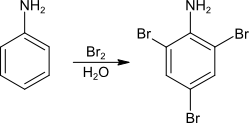
U anilinu - volné báze, je volný elektronový pár opět zapojen do konjugace s aromatickým systémem. Na aromatickém systému pak dochází k aktivaci ortho a para poloh. Elektrofilní substituci bromu na anilinu proto pozorujeme do ortho i para poloh.
- Závěr
-
Potvrdili jsme si vlastnosti aromatických aminů – rovnovážnou reakci s kyselinami na ve vodě rozpustné amoniové soli a zpětný převod na ve vodě nerozpustné aminy. Snadnost tvorby bromanilinu při elektrofilní aromatické substituci byla dokázána vylučováním žlutobílé sraženiny.