Biochemické vyšetření
Základní biochemické vyšetření
Hladina celkové bílkoviny je za normálního stavu asi 200x nižší než v séru. Za normálních okolností je 80 % celkové bílkoviny sérového původu, zbývajících 20 % je mozkového původu. Fyziologická hodnota celkové bílkoviny je při lumbální punkci 0,15–0,40 g/l. V mozkových komorách je hodnota celkové bílkoviny výrazně nižší. Novorozenci mají v likvoru vyšší hodnotu celkové bílkoviny pro nezralost hematolikvorové bariéry. Nejvyšší podíl v zastoupení celkové bílkoviny má albumin, v likvorovém prostoru jsou modifikovány dále některé sérové proteiny – např. prealbumin, transferin. Imunoglobuliny přestupují do likvoru z krve nebo vznikají intratékální syntézou v likvorových prostorách. K zánětlivým markerům dále patří haptoglobin, C-reaktivní protein, C3 a C4 složky komplementu, antitrombin III a α1-antitrypsin. K tumorovým markerům řadíme orosomukoid.
Klinický význam má zvýšení celkové bilkoviny, které nastává u zánětů (u bakteriálních zánětů výrazné zvýšení až na desítky gramů), poruchách cirkulace likvoru nebo u intratékální syntézy imunoglobulinů při aktivaci imunitního systému.
Glukóza
Je základním energetickým zdrojem pro nervovou tkáň, hladina glukózy v likvoru závisí na hladině glukózy v séru, tvoří asi 60 % sérové hodnoty. Vyšší výpovědní hodnotu má poměr CSF glukóza/S glukóza, který je za normálních poměrů 0,6. Klinický význam má snížení hladiny glukózy v likvoru nebo poměru glukózy v likvoru a séru. Doprovází bakteriální záněty, nádorové meningeální infiltrace, subarachnoideální krvácení.Laktát
Hladina laktátu v likvoru nezávisí na plazmatické koncentraci, laktát prakticky neprochází přes hematolikvorovou bariéru. Fyziologická hodnota laktátu je 1,2–2,1 mmol/l. Laktát vzniká při metabolismu glukózy bez přístupu kyslíku, klinický význam má jeho zvýšená hladina. Ke zvýšení dochází u zánětů, lehké zvýšení doprovází virové nebo tuberkulosní meningitidy. Výrazné zvýšení nastává u bakteriálních zánětů. Diskriminační hodnota pro rozlišení typu meningitidy je asi 4 mmol/l. Koncentrace laktátu bývá zvýšena u ischemických vaskulárních lézí.Chloridy
fyziologická hladina je 120–132 mmol/l, od jejich stanovení se upouští. Ke snížení chloridů dochází u výraznějších poruch hematolikvorové bariéry zejména u specifických zánětů jako je tuberkulózní meningitis.
Speciální biochemické vyšetření
Albumin
Albumin je syntetizován v játrech, do likvoru se dostává jedině přestupem přes hematolikvorovou bariéru. Slouží k posouzení funkčnosti této bariéry. Pro vyhodnocení poruchy funkce hematolikvorové bariéry má koncentrační kvocient CSF/sérum albumin vyšší senzitivitu než absolutní koncentrace albuminu v likvoru.
Z koncentrace albuminu v likvoru a séru vypočítáváme tzv. albuminový kvocient Q alb. = CSFalb./S alb. Hodnoty albuminového kvocientu závisí nejen na „propustnosti“ (permeabilitě) bariéry v užším slova smyslu, ale i na obratu (cirkulaci) likvoru. Závisí také na věku. Po narození je jeho hodnota zvýšená a postupně klesá asi do 3 měsíců věku a potom s věkem mírně stoupá. Normální hodnota Q albuminu je ve věkové kategorii 40 let asi 7,0.10-3. Mírně porušenou bariéru (což je vzestup Q albuminu asi o 1,5.10-3) nacházíme u chronických neuroinfekcí nebo roztroušené sklerózy. Střední poruchu bariéry (zvýšení hodnoty Q albuminu do dvojnásobku normální hodnoty) můžeme vidět např. u virových infekcí a těžká porucha bariéry (vyšší než dvojnásobek), je typická pro bakteriální meningitidy, polyradikuloneuritidu Guillain-Barrého typu, maligní meningeální infiltrace nebo herpetické encephalitidy. I při velmi vysokých hodnotách Q albuminu si hematolikvorová bariéra zachovává část své funkčnosti. Přestává plnit svou funkci až při metabolickém a energetickém rozvratu na úrovni membrán, tedy při stavech neslučitelných se životem.
Imunoglobuliny
Imunoglobuliny – zdrojem imunoglobulinů v likvoru je plazma, odkud imunoglobuliny přecházejí při poruše bariéry nebo intratékální syntéza v likvorovém prostoru při onemocnění CNS spojeném s imunitní reakcí.
Intratékální syntéza imunoglobulinů
Intratékální syntéza protilátek v centrálním nervovém systému pochází z perivaskulárních infiltrátů lymfocytů B, které lokálně proliferují, dozrávají v plazmocyty a produkují příslušné protilátky. Na rozdíl od známé a charakteristické reakce v séru, kde dochází k přechodu z protilátkové tvorby ve třídě IgM do třídy IgG v subakutní nebo chronické fázi nemoci, není takový přechod v intratékální syntéze přítomen. Tvorba protilátek ve třídě IgG/IgM/IgA je přítomna již na počátku onemocnění a zůstává relativně konstantní. Intratékální protilátková odpověď nemusí znamenat vždy akutní onemocnění, ale může být přítomna u zánětlivého onemocnění CNS, které se manifestuje zvýšeným počtem buněk v likvoru, dále u zbytkové intratékální syntézy po proběhlém onemocnění nebo u chronického zánětlivého autoimunitního procesu v CNS. Moderní likvorová diagnostika roztroušené sklerózy je dnes založena především na průkazu intratékální syntézy imunoglobulinů.
Kvantitativní určení intratékální syntézy imunoglobulinů
Zvýšení koncentrace imunoglobulinů v likvoru může být důsledkem jejich zvýšené koncentrace v séru, poruchy hematolikvorové bariéry nebo obou těchto faktorů. Dominantním transportním mechanismem přes hematolikvorovou bariéru je difúze proteinů ze séra do likvoru. Dle fyzikálních zákonů difúze prostupují větší molekuly pomaleji (např. IgM) než menší molekuly (např. IgG a albumin). Důsledkem zvýšení koncentrace určitého sérového proteinu je zvýšení koncentrace téhož proteinu v likvoru, avšak gradient vyjádřený poměrem koncentrace proteinu v likvoru a séru zůstává konstantní. Při porušené hematolikvorové bariéře dochází k patologickému zvýšení koncentrace proteinu v likvoru, proto je třeba stanovit albumin a příslušné imunoglobuliny současně v séru i v likvoru. Pro klinickou diagnostiku má nejvyšší význam stanovení intratékální syntézy IgG,IgM a IgA. K průkazu intratékální syntézy imunoglobulinů se v současné době doporučuje používat rovnici dle Reibera (2001), která popisuje vztah mezi Q albuminu a Q příslušného imunoglobulinu. Tento vztah není lineární, ale hyperbolický. Hranice mezi lokální syntézou imunoglobulinů a jejich pasivním přestupem je znázorněna modrou čárou. Hodnoty nad touto linií znamenají intratékální syntézu a rozsah je vyznačen přerušovanou čárou a vyjádřen v procentech. Vertikální přerušovaná čára odděluje normální a porušenou hematolikvorovou bariéru.
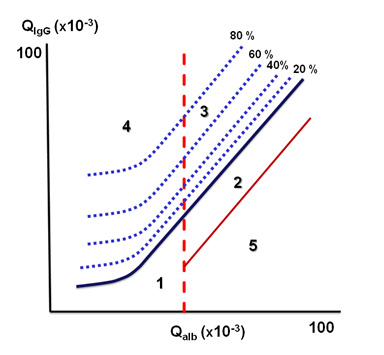
Obr. 23 Reibrův diagram
Interpretace patologických nálezů s ohledem na funkci hematolikvorové bariéry a intratékální syntézu:
- Oblast 1 – normální nález
- Oblast 2 – porucha funkce HLB bez intratékální syntézy
- Oblast 3 – porucha funkce HLB s intratékální syntézou imunoglobulinů
- Oblast 4 – intratékální syntéza se zachováním funkce HLB
- Oblast 5 – oblast analytických chyb
Z diagnostického hlediska lze na základě přítomnosti intratékální syntézy jednotlivých imunoglobulinů rozlišovat stavy
- bez průkazu intratékální syntézy Ig: časná bakteriální a virová meningitida, Guillainův-Barrého syndrom
- Intratékální syntéza s převahou IgG: roztroušená skleróza, neurolues, chronická HIV encefalitida.
- Intratékální syntéza s převahou IgA: neurotuberkulóza, mozkový absces
- Intratékální syntéza s převahou IgM: neuroborrelióza
Kvalitativní průkaz intratékální syntézy imunoglobulinů
Kvalitativní průkaz intratékální syntézy imunoglobulinů se provádí pomocí izoelektrické fokuzace (IEF) a následné imunochemické detekce imunoglobulinu třídy IgG. Současně je analogickým způsobem vyšetřeno sérum. Metoda izoelektrické fokuzace slouží k rozdělení látek amfoterní povahy (mají kyselé i bazické skupiny) a dělí se v gradientu pH podle svého izoelektrického bodu. Izoelektrický bod je pH, při kterém má bílkovina nulový náboj. Na základě mezinárodního konsensu je stanoveno pět typů rozdělení při IEF likvoru a séra.
- typ:normální stav bez průkazu oligoklonálních pásů (OP)
- typ: OP v likvoru, které nejsou v séru (zejména u roztroušené sklerózy)
- typ: OP v obou materiálech a navíc OP přítomné v likvoru (neuroborrelióza, mozkomíšní skleróza)
- typ: identické OP v likvoru a séru (paraneoplastické syndromy, SLE)
- typ: identické OP v likvoru a séru v úzkém gradientu (monoklonální gamapatie)
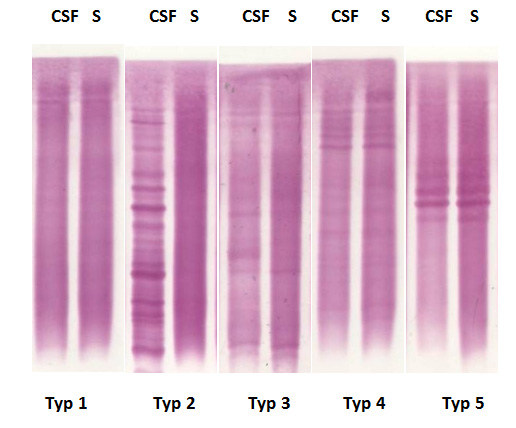
Obr. 24 Základní typy rozdělení při IEF
U pacientů s diagnózou roztroušené sklerózy je stanovení oligoklonálních pásů pozitivní až v 98 %. Oligoklonální pásy nacházíme i u infekčních procesů, u autoimunitních nebo systémových onemocnění.
Intratékální produkce specifických protilátek
Molekuly imunoglobulinů přecházejí z periferní krve do likvorových prostor i za fyziologických podmínek při neporušené funkci hematolikvorové bariéry. Porovnáním stanovení koncentrací celkového nespecifického imunoglobulinu v likvoru a séru s koncentracemi specifického imunoglobulinu (např. antiherpetického, antispalničkového, antiborreliového imunoglobulinu určité třídy) můžeme zjistit, zda koncentrační kvocient je u specifického imunoglobulinu stejný jako u celkového nespecifického IgG, nebo zda je vyšší. Pokud je vyšší, znamená to, že dochází k intratékální produkci specifických protilátek – tzn. vytváří se specifické protilátky přímo v CNS. Poměr těchto kvocientů se nazývá protilátkový index (AI) a za normální hodnoty se považují hodnoty 0,7–1,3. Hodnoty nad 1,4 jsou patologické a indikují intratékální syntézu specifických protilátek.
Významné výsledky v likvorové diagnostice roztroušené sklerózy přineslo zavedení specifické reakce MZR (morbilli, rubeola a varicella zoster), která umožňuje detekovat některá chronická onemocnění CNS již v době prvních klinických příznaků. Jako reakce MZR se označuje intratékální syntéza specifických protilátek třídy IgG proti neurotropním virům spalniček, zarděnek a planých neštovic. Přítomnost reakce MZR je vysvětlována moderní teorií imunitní sítě, ve které každá imunologická reakce indukovaná konkrétním antigenem postihuje celou imunitní síť. Kromě specifických protilátek proti vyvolávajícímu agens je zvýšena produkce mnoha dalších protilátek a autoprotilátek – tzv. polyspecifická imunitní odpověď. Koncentrace jednotlivých specifických protilátek v séru a likvoru jsou měřeny a vyjadřují se matematicky tzv. protilátkovým indexem (AI).